Wie wird der G-BA-Beschluss zum „Austausch von biotechnologisch hergestellten biologischen Fertigarzneimitteln durch Apotheken bei parenteralen Zubereitungen zur unmittelbaren ärztlichen Anwendung“ in der gelebten Praxis umgesetzt? Was ist noch ungeklärt?
Wir beantworten die wichtigsten Fragen.

Dafür stehen Wir!
Updates
Hersteller warnen vor Doppelbelastung
Walter Röhrer (Biogen) als Vorsitzender der AG Pro Biosimilars bestätigt
Automatische Substitution — Und Jetzt?
Pro Generika-Vorstand warnt vor Engpässen bei Krebs-Biologika
Von der Theorie in die Praxis: Was folgt aus dem G‑BA-Beschluss zur automatischen Substitution?
Diese 5 Punkte braucht es für einen starken Biosimilar-Standort
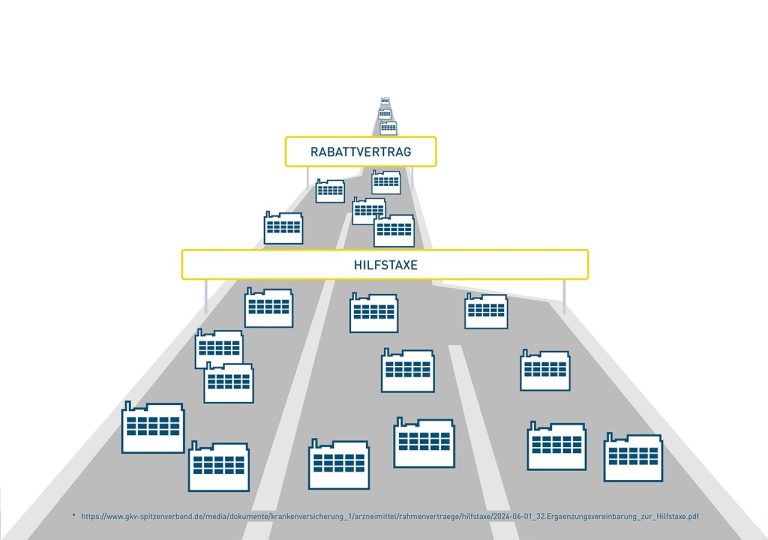
Seit dem 1.6.2024 droht eine gefährliche Doppelbelastung: Pharmazeutische Unternehmen unterliegen nicht nur der Hilfstaxe, sondern auch einem Rabattvertrag.
Gegen ihr Rheuma erhält Lynne ein Biopharmazeutikum. Wie das wirkt, was es verändert und warum es gut ist, dass es günstigere Nachahmerpräparate gibt, erklären wir hier.


Keinen Nutzen, hohe Risiken: Mehr Einsparungen sind bei Biosimilars nur auf Kosten der Versorgungssicherheit zu haben.